(Thethaovanhoa.vn) - Các hãng dược phẩm Pfizer của Mỹ và BioNTech của Đức ngày 28/9 cho biết họ đã bắt đầu đệ trình dữ liệu lên Cơ quan Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) để xin cấp phép tiêm chủng vaccine ngừa bệnh viêm đường hô hấp cấp COVID-19 của các hãng này cho trẻ em từ 5-11 tuổi.
Trong một tuyên bố, các hãng dược phẩm nói trên cho hay: “Những dữ liệu đã được chia sẻ với FDA để cơ quan này xem xét bước đầu. Một đơn chính thức xin cấp giấy phép sử dụng khẩn cấp (EUA) đối với vaccine ngừa COVID-19 cho trẻ em từ 5 tới dưới 12 tuổi dự kiến sẽ được đệ trình trong những tuần tới”.
Cũng theo tuyên bố này, những đơn xin cấp phép tương tự sẽ được đệ trình tới Cơ quan quản lý dược phẩm châu Âu (EMA) và các cơ quan khác.
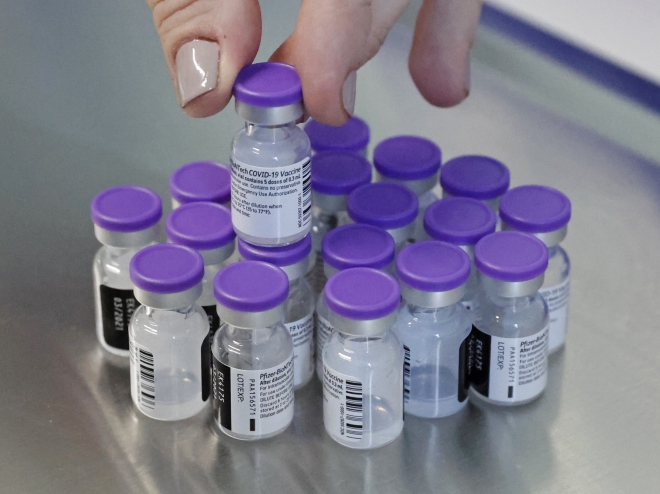
Thông tin trên được đưa ra một tuần sau khi hai hãng dược phẩm Pfizer và BioNTech thông cáo những kết quả khả quan từ một thử nghiệm lâm sàng toàn cầu cho thấy vaccine ngừa COVID-19 của họ an toàn và tạo ra phản ứng mạnh với những kháng thể trung hòa, qua đó giúp ngăn chặn virus SARS-CoV-2 xâm nhập vào tế bào.
- Hãng Pfizer/BioNTech xin cấp phép sử dụng vaccine Comirnaty cho trẻ em tại Mỹ
- FDA khuyến nghị tiêm liều tăng cường Pfizer cho người lớn tuổi
- BioNTech khẳng định Pfizer có tác dụng chống lại biến thể Delta
Trong thử nghiệm này, trẻ em từ 5-11 tuổi được áp dụng cơ chế tiêm 2 liều 10 microgam, so với 30 microgam đối với các nhóm tuổi lớn hơn. Các mũi tiêm cách nhau 21 ngày. FDA trước đây đã lưu ý rằng khi việc đệ trình chính thức được hoàn tất, cơ quan này sẽ hoàn thành việc xem xét "có thể trong vài tuần thay vì trong vài tháng".
Ngọc Ánh (P/v TTXVN tại Washington)
Tags

.jpg)